Bronquiolite Obliterante: Guia completo - Causas, sintomas, diagnóstico e tratamentos
Publicado em 9 de março de 2026 por Johann
Familiar de uma pessoa com BO
Também conhecido como: pulmão pop-corn · bronquiolite constritiva · PIBO · BOS · pulmão pop-corn
Atualizado em 9 de março de 2026 — Fontes: NCBI, PubMed, Orphanet, ERS/ATS/ISHLT, Frontiers in Pediatrics, RespiRare
Resumo
- Resumo: o que é bronquiolite obliterante?
- Definição médica
- Causas e fatores de risco
- Fisiopatologia: o que acontece nos pulmões
- Sintomas: como a doença se manifesta
- Diagnóstico: como confirmar a doença
- Classificação de gravidade (BOS pós-transplante)
- Tratamentos: opções terapêuticas atuais
- Prognóstico e evolução
- Prevenção: como reduzir os riscos
- Perspectivas de pesquisa e avanços recentes
- Perguntas frequentes (FAQ)
Resumo: o que é bronquiolite obliterante?
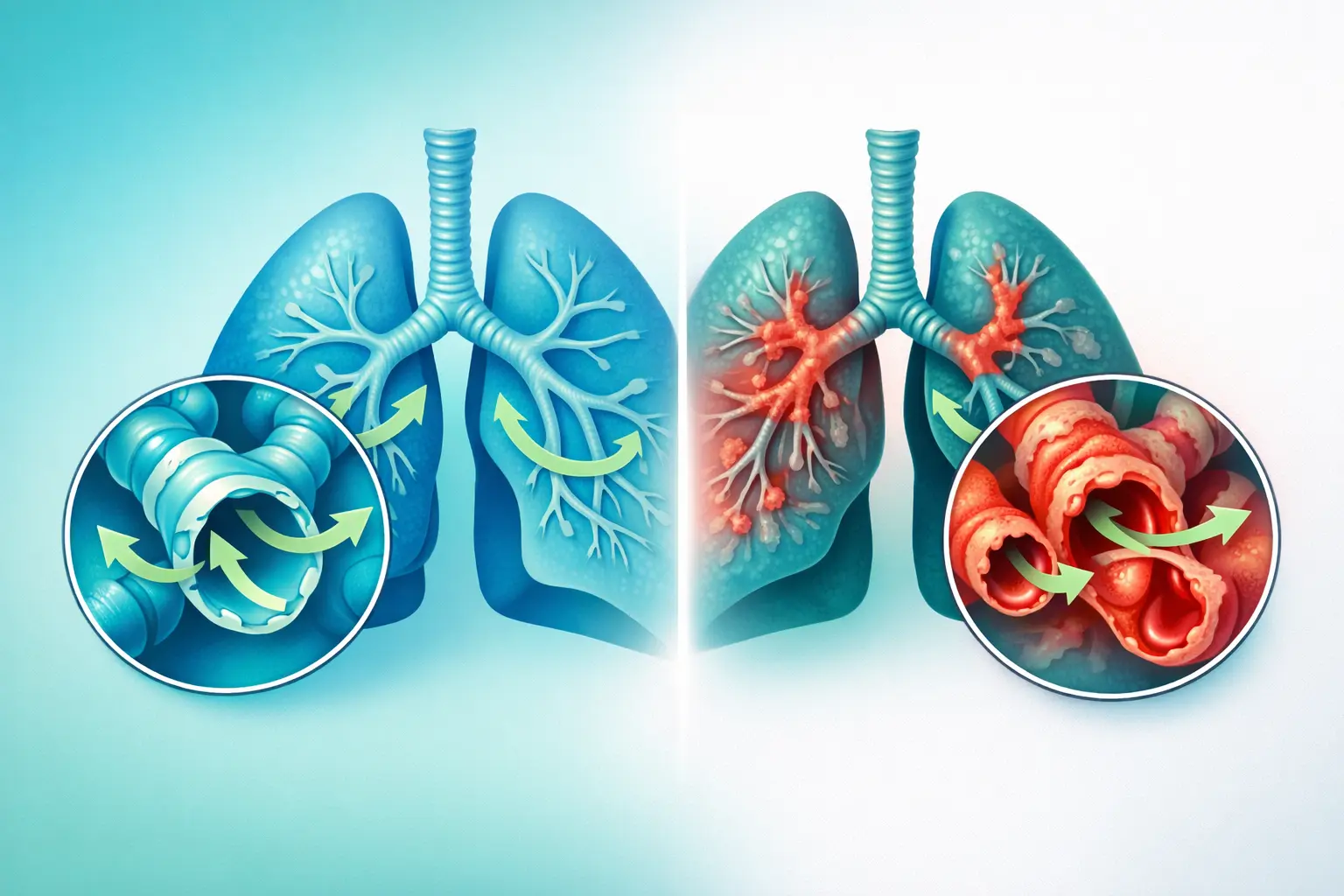
Para entender de forma simples: imagine seus pulmões como uma árvore. Os galhos grossos são os brônquios e, nas pontas, há milhares de pequenos galhos: são os bronquíolos . A bronquiolite obliterante ocorre quando esses pequenos galhos inflamam, cicatrizam e ficam progressivamente obstruídos. O ar tem cada vez mais dificuldade para circular. Respira-se com menos facilidade, tosse-se e cansa-se rapidamente. E, infelizmente, esses danos são, na maioria das vezes, irreversíveis .
É uma doença rara, crônica e grave. Ela pode afetar tanto crianças quanto adultos, mas por razões muito diferentes. Em crianças, ela ocorre mais frequentemente após uma infecção respiratória grave (chamada bronquiolite obliterante pós-infecciosa). Em adultos, está frequentemente associada a um transplante de órgão (pulmão ou medula óssea), à inalação de substâncias tóxicas ou a certas doenças autoimunes.
O apelido “pulmão de pipoca” (ou “popcorn lung”) vem de uma história marcante: no início dos anos 2000, nos Estados Unidos, trabalhadores de fábricas de pipoca desenvolveram essa doença após inalarem durante anos um produto químico, o diacetil, que dava sabor de manteiga à pipoca. Hoje, essa ligação também foi mencionada em relação a certos aromas de cigarros eletrônicos, embora nenhum caso de bronquiolite obliterante diretamente relacionado ao vaporizador tenha sido confirmado até o momento em consumidores individuais.
Em outras palavras: não se trata da bronquiolite clássica do bebê (que é aguda e viral), mas de uma doença pulmonar crônica e muito mais grave.
Definição médica de bronquiolite obliterante
A bronquiolite obliterante (BO), também conhecida como bronquiolite constritiva ou bronquiolite obliterante crônica, é uma patologia pulmonar obstrutiva caracterizada por uma inflamação transmural e circunferencial dos bronquíolos terminais e respiratórios. Essa inflamação evolui para uma fibrose peribronquiolar com estreitamento progressivo — ou mesmo obliteração completa — da luz das pequenas vias aéreas, poupando os espaços alveolares e o parênquima pulmonar distal.
Classificada como doença rara pela Orphanet (código ORPHA:1303), a OB foi descrita pela primeira vez com esse termo por Reynaud em 1835 e claramente caracterizada na literatura científica a partir de 1981. Sua incidência exata na população geral ainda é difícil de determinar, mas ela afeta uma proporção significativa de pacientes transplantados: cerca de 75% dos receptores de transplante pulmonar em 10 anos e entre 5% e 14% dos receptores de transplante de células-tronco hematopoiéticas.
Atenção à terminologia: a bronquiolite obliterante (BO) não deve ser confundida com a bronquiolite obliterante com pneumonia organizada (BOOP), agora chamada de pneumonia organizada criptogênica (COP) . São duas entidades clínicas e histológicas distintas. A BOOP/COP afeta os alvéolos, além dos bronquíolos, e geralmente responde bem aos corticosteroides, enquanto a BO é uma lesão estritamente bronquiolar, muitas vezes refratária ao tratamento.
Causas e fatores de risco
As causas da bronquiolite obliterante são múltiplas. Distinguem-se classicamente quatro grandes categorias etiológicas.
1. Bronquiolite obliterante pós-infecciosa (PIBO)
É a forma mais frequente em crianças. Surge após uma infecção respiratória grave que danifica o epitélio dos bronquíolos, desencadeando uma resposta inflamatória e fibrosa que leva à obstrução das pequenas vias aéreas.
Os principais agentes patogênicos envolvidos são:
- Adenovírus (sorotipos 3, 7, 11, 21 e, mais recentemente, 55) — responsável por 20 a 69% dos casos de PIBO. Até 28% das crianças que sobreviveram a uma pneumonia grave por adenovírus podem desenvolver PIBO.
- Mycoplasma pneumoniae — cada vez mais envolvido, especialmente em crianças mais velhas, com incidência crescente na Ásia.
- Vírus sincicial respiratório (VSR), influenza, citomegalovírus, HIV, HHV-8.
- Infecções bacterianas e fúngicas mais raramente.
Os fatores de risco identificados para o desenvolvimento de PIBO após pneumonia por adenovírus incluem: hipoxemia, sibilância persistente, uso de ventilação mecânica, internação hospitalar prolongada e duração da febre.
Fato notável: o diagnóstico de PIBO é frequentemente consideravelmente retardado. A literatura relata um intervalo médio entre o aparecimento dos sintomas e o diagnóstico que varia de 15 a 88 meses. Esse atraso se deve à semelhança dos sintomas com o asma não controlada.
2. Síndrome de bronquiolite obliterante pós-transplante (BOS)
É a principal causa de falha a médio e longo prazo do transplante pulmonar. A BOS é considerada uma forma de rejeição crônica do enxerto. Mais de 50% dos receptores desenvolvem algum grau de BO em 5 anos, com um intervalo médio de diagnóstico de 16 a 20 meses.
Após um transplante de células-tronco hematopoiéticas (alogênese de medula óssea), a BO ocorre em 5 a 14% dos casos e constitui uma manifestação da doença do enxerto contra o hospedeiro (GVH) crônica. O risco é avaliado em cerca de 14% nos pacientes que desenvolvem GVH crônica.
Os fatores de risco incluem: episódios de rejeição celular aguda, presença de anticorpos anti-HLA, refluxo gastroesofágico com microaspirações, tabagismo e certas infecções virais que ocorrem nos primeiros 100 dias após o transplante.
3. Bronquiolite obliterante de origem tóxica ou profissional
A inalação de substâncias químicas irritantes pode causar BO. Os agentes tóxicos mais documentados incluem: diacetil (aroma de manteiga), dióxido de enxofre, dióxido de nitrogênio (silos agrícolas), amônia, cloro, cloreto de tionila, isocianato de metila, fluoreto de hidrogênio, fosgênio, gás mostarda e ozônio.
O caso emblemático do diacetil e do “pulmão de pipoca”: no início dos anos 2000, o NIOSH documentou casos de BO em trabalhadores de uma fábrica de pipoca no Missouri, expostos massivamente a vapores de diacetil. Este composto (C₄H₆O₂), naturalmente presente na manteiga e no queijo, provoca inflamação crônica dos bronquíolos quando inalado em grandes quantidades ao longo do tempo.
A ligação com o vaporizador: em 2015, um estudo da Universidade de Harvard detectou a presença de diacetil em alguns e-líquidos aromatizados. Em 2019, o Canadian Medical Association Journal relatou um caso em um usuário de vaporizador. No entanto, até o momento, nenhuma série de casos estabeleceu formalmente que o vaporizador causava BO em populações. Na França e na Europa, a maioria dos fabricantes retirou o diacetil de seus produtos. No entanto, recomenda-se cautela: mais de 180 agentes aromatizantes usados em e-líquidos nunca foram testados para inalação.
4. Bronquiolite obliterante associada a doenças autoimunes
Várias doenças sistêmicas estão associadas ao desenvolvimento de BO: poliartrite reumatoide (a mais frequente), lúpus eritematoso sistêmico, doenças inflamatórias intestinais, síndrome de Stevens-Johnson, pênfigo paraneoplásico e, mais raramente, artrite juvenil idiopática ou nefropatia por IgA.
Em casos raros, nenhuma etiologia pode ser identificada: fala-se então de bronquiolite obliterante idiopática ou criptogênica.
Fisiopatologia: o que acontece nos pulmões
O mecanismo patogênico da BO segue um padrão comum, independentemente da causa inicial, embora algumas especificidades variem de acordo com a etiologia.
Fase 1 — Agressão inicial: uma lesão danifica as células epiteliais dos bronquíolos terminais e respiratórios. Essa agressão pode ser infecciosa, química, imunológica ou isquêmica. Ela provoca uma necrose localizada do epitélio bronquiolar.
Fase 2 — Resposta inflamatória desregulada: a inflamação das estruturas subepiteliais leva a um acúmulo de exsudato fibrinopurulento na luz bronquiolar. Observa-se uma infiltração por linfócitos, neutrófilos e macrófagos. As citocinas pró-inflamatórias (IL-8, IFN-γ) estão significativamente elevadas.
Fase 3 — Fibroproliferação: a denudação da mucosa expõe os miofibroblastos da submucosa, que proliferam excessivamente. Esse processo de reparação aberrante leva ao depósito de colágeno e mucopolissacarídeos ácidos, estreitando progressivamente a luz bronquiolar.
Fase 4 — Fibrose e obliteração: o tecido fibroso preenche parcial ou totalmente a luz das pequenas vias aéreas, causando uma obstrução fixa e irreversível. Às vezes, pólipos intraluminais (corpos de Masson) se formam pela proliferação de histiócitos e capilares.
No contexto pós-transplante pulmonar, o mecanismo envolve especificamente insuficiência microvascular e respostas alogênicas dirigidas contra o enxerto.
Do ponto de vista histopatológico, distinguem-se dois tipos: o tipo constritivo (fibrose peribronquiolar com compressão externa) e o tipo proliferativo (obstrução intraluminal por pólipos de tecido de granulação). Essas duas formas podem coexistir.
Sintomas: como a doença se manifesta
A bronquiolite obliterante é uma doença insidiosa. Os sintomas são frequentemente pouco específicos no início, o que explica os erros e atrasos frequentes no diagnóstico. Eles geralmente aparecem 2 a 8 semanas após a agressão inicial e, em seguida, agravam-se progressivamente.
Os principais sintomas incluem:
- Dispneia progressiva: inicialmente ao esforço (subir escadas, correr), depois em repouso nas formas avançadas. É frequentemente o primeiro sinal.
- Tosse seca persistente: não produtiva, que não responde aos tratamentos clássicos para tosse ou asma.
- Sibilância (chiado no peito): principalmente ao expirar.
- Fadiga crônica: diminuição da tolerância ao esforço.
- Broncorreia: aumento da secreção de muco brônquico nos estágios avançados.
- Hipoxemia tardia: diminuição progressiva da saturação de oxigênio no sangue.
Em crianças, em particular: os sintomas persistem por mais de 6 semanas após uma infecção aguda grave, com taquipneia, tosse crônica com muco e estertores difusos à auscultação. A criança, que até então era saudável, não recupera seu estado respiratório normal.
⚠️ Atenção — Armadilha diagnóstica: a OB é frequentemente confundida com asma não controlada, DPOC ou uma simples “tosse pós-infecciosa”. A diferença crucial é que a obstrução brônquica na OB é fixa e não reversível com broncodilatadores, ao contrário da asma.
Diagnóstico: como confirmar a doença
O diagnóstico da bronquiolite obliterante baseia-se em um conjunto de argumentos clínicos, funcionais e radiológicos.
Entrevista e exame clínico
O médico procura um histórico de exposição (infecção grave, transplante recente, exposição profissional), uma cronologia compatível e sintomas persistentes não reversíveis. A auscultação pode revelar sibilos expiratórios e/ou estertores.
Testes funcionais respiratórios (TFR)
A espirometria mostra um distúrbio ventilatório obstrutivo caracterizado por uma diminuição do VEMS (volume expiratório máximo por segundo), não reversível com broncodilatadores. A relação VEMS/CVF está reduzida. A medição do DEM 25-75 pode ser alterada precocemente.
Tomografia computadorizada de alta resolução do tórax (TCAR)
Este é o exame de imagem fundamental. Os sinais característicos incluem: um aspecto denominado “mosaico” da perfusão, aprisionamento aéreo visível nas cortes expiratórias, espessamento das paredes bronquiolares e, por vezes, bronquiectasias centrais.
Broncoscopia e lavagem broncoalveolar (LBA)
A BAL frequentemente mostra neutrofilia elevada (46% a 90% das células). Ela também permite excluir uma infecção ativa.
Biópsia pulmonar
A biópsia pulmonar cirúrgica continua sendo o “padrão ouro” para o diagnóstico definitivo. Ela mostra inflamação peribronquiolar, fibrose e obliteração da luz. No entanto, é invasiva e sujeita a erros de amostragem. As diretrizes internacionais (ISHLT/ATS/ERS) agora permitem o diagnóstico de BOS com base no declínio do VEMS sem biópsia.
Outros exames complementares
Um ECG pode procurar sinais de hipertensão pulmonar. A oximetria noturna pode revelar dessaturações. Exames laboratoriais permitem descartar outras causas.
Ferramenta clínica de previsão (Colom & Teper) para PIBO: uma pontuação baseada em três variáveis — histórico típico de bronquiolite grave em uma criança anteriormente saudável, exposição documentada ao adenovírus e aspecto em mosaico na tomografia computadorizada de alta resolução — permite suspeitar precocemente do diagnóstico. Uma pontuação ≥ 7 sugere um risco elevado de PIBO.
Classificação de gravidade (BOS pós-transplante)
A ISHLT (Sociedade Internacional para Transplante Cardíaco e Pulmonar) definiu estágios de gravidade com base na porcentagem de declínio do VEMS em relação ao melhor valor pós-transplante.
| Estágio BOS | VEMS em relação ao melhor valor | Significado |
|---|---|---|
| BOS 0 | > 90% | Normal |
| BOS 0-p | 81–90 % e/ou DEM25-75 ≤ 75 % | Potencial (alerta precoce) |
| BOS 1 | 66–80 | Leve |
| BOS 2 | 51–65% | Moderado |
| BOS 3 | ≤ 50% | Grave |
Cada estágio é subdividido em “a” (sem documentação histológica) e “b” (com biópsia confirmando a BO).
Tratamentos: opções terapêuticas atuais
⛔ Informação essencial: a bronquiolite obliterante é uma doença irreversível e crônica. Não existe tratamento curativo. O objetivo terapêutico é retardar a progressão, aliviar os sintomas e prevenir complicações.
Supressão do agente causador
Em caso de exposição tóxica profissional, a primeira medida é a interrupção imediata da exposição. Após o transplante, a otimização da imunossupressão é a prioridade.
Tratamentos medicamentosos
- Corticoides: sistêmicos (prednisona, metilprednisolona) e/ou inalados (fluticasona). Bolus IV de metilprednisolona (20-30 mg/kg durante 3 dias consecutivos, repetidos mensalmente durante 3 a 6 meses) são usados em crianças com PIBO, com melhora clínica na maioria dos casos.
- Azitromicina: antibiótico macrolídeo com propriedades anti-inflamatórias e imunomoduladoras. Tratamento padrão na BOS pós-transplante. Na profilaxia, reduziria a prevalência da BOS. Alertas recentes mostraram um risco potencial de mortalidade excessiva por recidiva tumoral em certos contextos, exigindo uma avaliação cautelosa.
- Imunossupressores: ciclofosfamida, tacrolimus, ciclosporina — usados principalmente nas formas autoimunes ou pós-transplante.
- Broncodilatadores inalatórios: eficácia limitada (obstrução fixa), mas possível alívio sintomático parcial.
- Montelukast: antagonista dos leucotrienos, cada vez mais utilizado como adjuvante (trifarmacoterapia FAM: fluticasona, azitromicina, montelukast).
- Terapias direcionadas (perspectivas): os inibidores de citocinas pró-inflamatórias são uma via de pesquisa promissora.
Tratamentos não medicamentosos
- Oxigenoterapia: em casa em caso de hipoxemia crônica, especialmente noturna ou durante o esforço.
- Reabilitação pulmonar: programas estruturados de exercícios e educação terapêutica.
- Fotoforese extracorpórea (ECP): técnica emergente no BOS refratário pós-transplante, resultados encorajadores.
- Radioterapia linfóide (exploratória): resultados preliminares encorajadores, mas nível de evidência ainda baixo.
- Transplante pulmonar: opção de último recurso em formas terminais, incluindo o retransplante.
Prognóstico e evolução
O prognóstico depende fortemente da etiologia, da gravidade no momento do diagnóstico e da resposta ao tratamento.
- PIBO em crianças: prognóstico mais favorável do que as formas pós-transplante. Baixa mortalidade, mas alta cronicidade. Cerca de 68% das crianças têm uma evolução favorável. Em casos raros, pode ocorrer reabsorção parcial. As formas relacionadas ao síndrome de Stevens-Johnson são frequentemente progressivas.
- BOS pós-transplante pulmonar: prognóstico mais sombrio. A probabilidade de permanecer livre de BOS em 5 anos é de apenas 36%. A sobrevida pós-BOS é de cerca de 51% em 3 anos. O risco de morte é multiplicado por cerca de 6.
- BO associada a doenças autoimunes: a imunossupressão pode estabilizar o estado clínico. Evolução variável.
- BO de origem tóxica: frequentemente estabiliza após a interrupção da exposição, mas geralmente não regrediu.
Sem tratamento, a evolução natural tende para uma insuficiência respiratória crônica progressiva, que pode ser fatal.
Prevenção: como reduzir os riscos
- Vacinas em dia: gripe anual, vacina antipneumocócica, imunoprofilaxia anti-VRS (palivizumabe) para bebês em risco.
- Tratamento rápido de infecções respiratórias: especialmente em crianças, para limitar os danos bronquiolares.
- Proteção respiratória no ambiente profissional: equipamentos adequados durante a exposição a agentes químicos voláteis.
- Parar de fumar e evitar o tabagismo passivo: fator agravante importante.
- Monitoramento rigoroso pós-transplante: espirometria regular e tratamento profilático com azitromicina.
- Cuidado com o cigarro eletrônico: dar preferência a e-líquidos certificados sem diacetil ou substitutos suspeitos.
- Evitar qualquer contato infeccioso: especialmente para pacientes imunodeprimidos ou transplantados.
Perspectivas de pesquisa e avanços recentes
Biomarcadores precoces: a identificação de marcadores biológicos que permitam o diagnóstico antes do estabelecimento da fibrose é um desafio importante. As citocinas IL-8 e IFN-γ, bem como a LDH sérica, estão elevadas nas formas pós-adenovirais e são objeto de estudos preditivos.
Microbioma pulmonar: estudos sobre o BOS pós-transplante demonstraram que a disbiose microbiana está associada a um risco aumentado de BO e a uma evolução mais desfavorável.
Consenso internacional chinês 2023: a China publicou uma reformulação do consenso de especialistas sobre o diagnóstico e tratamento da BO em crianças, integrando os recentes avanços no diagnóstico precoce e estratégias terapêuticas.
Roteiro ERS/EBMT 2025: um grupo de trabalho internacional publicou um roteiro para melhorar o rastreamento precoce da BO pós-aloenxerto, com propostas para redefinir os critérios diagnósticos.
Modelos preditivos e nomogramas: nomogramas clínicos permitem prever o prognóstico da POBO desde o diagnóstico, com base na função pulmonar inicial e nos sinais de inflamação bronquiolar.
Perguntas frequentes (FAQ)
O que é bronquiolite obliterante em termos simples?
É uma doença em que as vias respiratórias mais pequenas dos pulmões (os bronquíolos) inflamam, cicatrizam e ficam progressivamente obstruídas. O ar circula cada vez com mais dificuldade, o que provoca falta de ar crónica. Infelizmente, os danos são irreversíveis na maioria dos casos.
Quais são as principais causas?
As quatro principais causas são: infecções respiratórias graves (principalmente adenovírus em crianças), transplantes de órgãos (pulmão, medula óssea), inalação de substâncias tóxicas (diacetil, gases químicos industriais) e certas doenças autoimunes (poliarterite reumatoide, lúpus).
A bronquiolite obliterante tem cura?
Não, é uma doença irreversível. Os tratamentos (corticoides, azitromicina, imunossupressores, oxigenoterapia) visam retardar a progressão e aliviar os sintomas. Nos casos mais graves, pode ser considerada uma transplantação pulmonar.
Qual é a relação entre o vaporizador e o pulmão pop-corn?
O diacetil, um aroma que confere um sabor amanteigado, foi detectado em alguns e-líquidos. É conhecido por causar BO em trabalhadores expostos em grande escala. No entanto, nenhum caso formal de BO diretamente causado pelo vaporizador foi confirmado em grande escala. Na Europa, a maioria dos fabricantes retirou o diacetil de seus produtos.
Qual é a diferença em relação à bronquiolite do lactente?
A bronquiolite aguda do lactente é uma infecção viral frequente (frequentemente VRS), geralmente benigna e que cura em poucas semanas. A bronquiolite obliterante é uma doença crônica, rara e grave, com danos permanentes nos pulmões. São duas patologias muito diferentes, apesar do nome semelhante.
Como se diagnostica a bronquiolite obliterante?
O diagnóstico baseia-se na combinação de um histórico compatível, testes funcionais respiratórios que mostram uma obstrução fixa não reversível, uma tomografia computadorizada torácica de alta resolução (aspecto em mosaico, retenção de ar) e, às vezes, uma biópsia pulmonar.
É possível prevenir a bronquiolite obliterante?
Algumas medidas reduzem o risco: vacinas em dia (gripe, pneumococo, VRS), tratamento rápido de infecções respiratórias em crianças, proteção respiratória profissional, parar de fumar, acompanhamento regular pós-transplante e cautela com e-líquidos aromatizados.
Fontes e referências
- StatPearls / NCBI — Bronquiolite obliterante
- Orphanet — Bronquiolite obliterante (ORPHA:1303)
- ISHLT/ATS/ERS — Diagnóstico e tratamento da BOS (2014)
- RespiRare — Bronquiolite obliterante não relacionada a transplante
- Associação Pulmonar do Quebec
- Frontiers in Pediatrics — Fatores de risco PIBO/adenovírus (2024)
- Canadian Respiratory Journal — BO pós-infecciosa em crianças (2025)
- Canadian Respiratory Journal — Relatório do workshop sobre PIBO (2020)
- European Lung Foundation — Tratamento da cGvHD pulmonar
- National Jewish Health — Bronquiolite obliterante
Aviso: este artigo é fornecido apenas para fins informativos e educacionais. Ele não substitui, em hipótese alguma, uma consulta médica. Se você ou seu filho apresentarem sintomas respiratórios persistentes, consulte um médico ou pneumologista.